728x90
반응형
[단독] 미코바이오메드 “원숭이두창 국내 상륙 시 진단키트 본격 공급
2021년 1월 질병청과 공동특허 등록
2020년 4월 진단기기 개발 완료
질병청 “국내 유입 가능성도 배제 못해”
2016년 검사체계 구축…검사 확대 검토
미코바이오메드(214610)는 전 세계적으로 확산하고 있는 ‘원숭이두창’의 국내 감염 의심자가 나오면 즉시 진단기기를 공급할 계획이다. 이 회사는 국내에서는 유일하게 원숭이두창을 검출할 수 있는 체외진단의료기기 기술을 보유하고 있다. 2020년 4월 관련 진단기기 개발을 완료했으며 지난해 1월 질병관리청과 원숭이두창 특허를 공동출원했다.
미코바이오메드 관계자는 24일 “질병관리청과 함께 특허를 공동출원한 만큼 요청이 오면 언제든지 생산을 확대해 적극적으로 대응할 것”이라며 “만약 국내에서도 원숭이두창 감염자가 발생하면 질병청 주체로 진행되는 유전자증폭검사(PCR)에서 미코바이오메드 제품이 사용될 것이 확실하다"고 말했다.
미코바이오메드는 질병청과 함께 원숭이두창 등 15종의 병원체를 검출할 수 있는 실시간 유전자 검사 특허를 2019년 출원했고, 지난해 1월 5일자로 등록을 마쳤다. 2020년 4월에는 희귀 감염병을 진단할 수 있는 진단기기 개발과 관련한 질병청 용역과제를 완료하기도 했다. 당시 연구과제를 통해 원숭이두창을 포함해 브루셀라, 보툴리눔균 등 약 33가지 병원체를 검출할 수 있는 시약 및 진단기기를 개발해 보유하고 있다.
이 같은 성과에 힘입어 미코바이오메드는 이날 오후 2시 7분 기준 2.27% 오른 8111원대에 거래 중이다. 거래량은 384만 6592주에 달한다. 전날에는 14.93% 오른 7930원에 거래를 마쳤다.
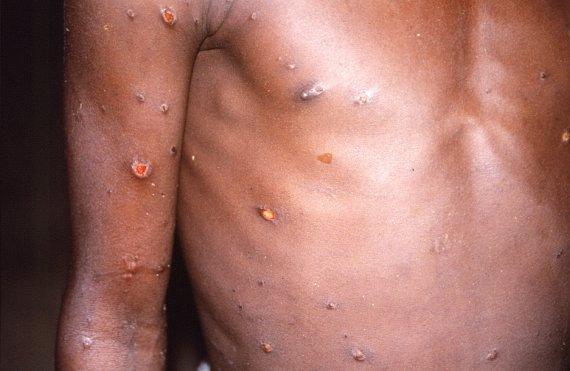
원숭이두창은 발열·오한·두통과 함께 손에 수두와 유사한 수포성 발진이 퍼지는 것이 특징인 바이러스성 질환이다. 잠복기는 통상 6~13일, 최장 21일까지로 알려져 있다. 방역대책본부(방대본)는 이날 영국, 포르투갈, 스페인, 스웨덴, 미국, 캐나다, 이스라엘, 호주 등 18개국에서 발생했으며 171명이 감염됐다고 밝혔다. 의심 증상자도 86명 나온 상태다.
아직 국내에는 유입되지 않았지만 유입 가능성을 배제할 수는 없는 상황이다. 방대본은 “원숭이두창은 사람 간 감염이 드문 것으로 평가되지만 해외여행 증가와 잠복기를 고려할 때 해외 유입 가능성을 배제할 수 없다”면서 “원숭이두창 발생 국가를 방문하고 온 여행객을 대상으로 입국시 발열체크와 건강상태 질문서를 받고 있다”고 말했다. 이어 “지난 2016년 원숭이두창에 대한 검사체계를 이미 구축했다”며 “국내 발생에 대비해 전국 시도 보건환경연구원에서의 검사 확대도 검토하고 있다”고 설명했다.
현대바이오, FDA에 '원숭이두창' 치료제 패스트트랙 신청한다
'애니멀 룰' 적용시 동물효능실험만으로 원두치료제 승인 가능
美연구진 "원숭이두창에 효능 1위 후보약은 니클로사마이드"
美연구진 "원숭이두창에 효능 1위 후보약은 니클로사마이드"

현대바이오가 최근 세계적 팬데믹(대유행) 조짐을 보이는 원숭이 두창(monkeypox, 이하 원두) 사태 해결을 위해 자사의 범용 항바이러스제 후보약물을 들고 미국으로 직행한다고 24일 밝혔다.
현대바이오는 신종 코로나바이러스 감염증(코로나19) 치료를 위해 먹는 항바이러스제로 개발한 CP-COV03를 원숭이 두창 치료제로 사용할 수 있도록 미국 식품의약국(FDA)에 패스트 트랙(fast track)을 신청하기로 결정했다.
현대바이오는 미국 현지의 바이오 분야 전문 로펌을 통해 CP-COV03가 '동물실험갈음규정'(Animal Rule) 적용으로 패스트 트랙이 가능하다는 사실을 확인하고 이 같이 결정했다. 동물실험갈음규정은 미국 등 주요국이 천연두나 원두처럼 사람을 대상으로 한 임상시험이 불가능하거나 비윤리적일 경우 동물실험 결과만으로 치료제로 승인하는 제도로, 일종의 패스트 트랙 절차다. FDA는 2018년 미 제약기업인 시가 테크놀로지가 동물실험을 거쳐 천연두 치료용으로 개발한 '티폭스'(TPOXX)를 천연두 치료제로 승인한 것을 비롯해 지금까지 13종의 약물에 애니멀 룰을 적용해 신약으로 승인한 바 있다.
회사 측은 FDA에 CP-COV03의 그간 동물실험 결과 등 관련 자료도 신속히 제출하기로 했다.
CP-COV03의 주성분인 니클로사마이드는 원두 바이러스에 효능이 탁월하다는 학계의 실험결과도 이미 나와 있다.
미 캔자스대 연구진은 니클로사마이드가 1마이크로몰의 낮은 농도에서도 원두 바이러스와 같은 계열인 백시니아 바이러스 증식을 무려 100분의 1 수준으로 낮추는 효능을 발휘한 세포실험 결과를 2020년 7월 국제학술지인 '백신즈'(vaccines)를 통해 공개한 바 있다. 연구진은 총 3228종의 현존 약물을 대상으로 약효 표적을 세포로 하고, 내성을 일으키지 않으면서 효능을 발휘하는 약물을 찾기 위한 실험을 진행한 끝에 4종의 후보를 찾았는데 이 중 FDA 승인을 받은 것은 니클로사마이드가 유일했다.
FDA가 애니멀 룰을 적용할 경우 그간 동물실험에서 약물의 안전성이 검증된 CP-COV03는 현재 진행 중인 코로나19 임상2상에서 혈중유효약물농도(PK)와 안전성이 확인되면 원두에 감염된 동물 효력실험을 통해 원두 치료제로 곧바로 승인받을 수 있다.
이에 따라 현대바이오는 CP-COV03의 코로나19 임상2상의 신속한 진행을 위해 내주부터 임상수행병원을 확대하는 등 임상진행 속도 제고에 박차를 가하기로 했다.
약효가 세포를 표적하는 니클로사마이드 기반의 CP-COV03는 바이러스가 침입하면 세포가 그 바이러스를 이물질로 인식, 제거하도록 하는 세포의 오토파지(autophagy, 자가포식) 작용을 촉진하는 범용 항바이러스제 후보물질로, 약리작용 메커니즘이 모든 바이러스에 적용 가능하다는 과학계의 평가를 받아왔다.
현대바이오 오상기 대표는 "CP-COV03는 모든 바이러스 제거가 가능한 메커니즘의 니클로사마이드를 주성분으로 개발한 범용 항바이러스제"라며 "FDA의 패스트 트랙으로 CP-COV03가 원두 치료제가 되면 20세기 대표적 범용 항생제인 페니실린처럼 혁신적인 항바이러스제가 탄생하는 것"이라고 의미를 부여했다.
728x90
'건강상식과 정보' 카테고리의 다른 글
| 과일채소안전한보관법 (18) | 2022.05.29 |
|---|---|
| 여름철대상포진에좋은식품 (55) | 2022.05.28 |
| 여름철보양식품 (48) | 2022.05.27 |
| 폭식후에먹으면좋은음식 (10) | 2022.05.25 |
| 뇌를깨우는음료 (16) | 2022.05.24 |
| 우울증에좋은운동과식품 (15) | 2022.05.23 |
| 무더운여름철에좋은보양음식 (13) | 2022.05.22 |
| 면역력에 좋은식품 (12) | 2022.05.21 |